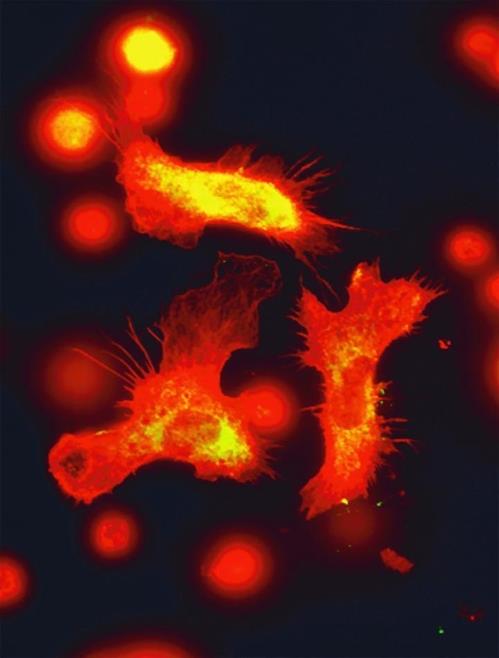
![림프절의 암세포<br>
림프절에서 항산화 코팅을 받는 흑색종 세포 이미지.<br>
이렇게 '지방 코팅'을 거친 암세포는 산화 스트레스를 잘 견뎌 멀리 떨어진 부위에 전이할 확률이 높다.<br>
[미 UTSW 제공 / 재판매 및 DB 금지]](http://www.hmj2k.com/data/photos/20201147/art_16056076979825_94cdfa.jpg)
폐는 전이암이 가장 많이 생기는 부위로 꼽힌다.
원발 암에서 떨어져 나와 혈액을 타고 몸 안을 돌던 암세포 무리는 허파꽈리(air sacs)를 둘러싼 미세혈관에 걸려 뿌리를 내리곤 한다.
허파꽈리의 미세혈관은, 산소가 적혈구에 잘 전달되게 하기 위해 복잡하게 갈라진 구조로 돼 있다.
다른 부위에서 옮겨온 암세포가 일단 폐에 터를 잡으면 다양한 화학신호를 내보내 인체의 면역 반응 유도를 방해한다.
하버드대 연구진이 적혈구를 이용해 면역세포 유도 물질을 직접 폐 전이암에 투입하는 획기적인 약물 전달법을 개발했다.
'EASI(적혈구 고정 조직 면역치료)'로 명명된 이 치료법은 동물 실험에서 유방에서 폐로 전이된 종양의 성장을 멈추게 할 뿐 아니라, 암의 재발을 막는 백신 작용도 유도했다.
이 연구는 하버드대 부설 와이스 생체모방(Biologically Inspired) 공학 연구소와 존 A 폴슨 공학 응용과학 대학의 과학자들이 함께 수행했다.
관련 논문은 저널 '네이처 생의학 공학(Nature Biomedical Engineering)'에 최근 실렸다.
약물을 담은 나노 입자를 적혈구에 붙임으로써 간이나 지라의 혈액 여과를 피하게 한 것이다.
이렇게 하면 나노 입자가 혈액 안에서 충분히 오래 견딜 뿐 아니라, 과잉 투여에 따른 약물 독성 피해도 최소화할 수 있다.
연구팀은 이 기술을 화학 치료제 대신 폐 전이암에 쓸 수 있는지 확인하기 위해 CXCL 10이라는 케모카인(chemokine), 즉 백혈구 유도 저분자 단백질로 실험을 진행했다.
폐 전이암은 주변 환경에서 이런 케모카인을 제거해 자신을 공격할 수 있는 백혈구 유인 신호를 미리 차단한다.
연구팀은 '이뮤노베이트(ImmunoBait)'로 명명한 CXCL10 나노입자를, 폐 전이 유방암을 가진 생쥐의 적혈구에 붙여 수혈했다.
연구팀은 폐 혈관 세포(ICAM-1) 단백질에 달라붙는 성질을 가진 항체로 이뮤노베이트의 표면을 처리했다.
이렇게 보강된 이뮤노베이트는 EASI 투여 후 6시간까지 생쥐의 폐에 머물면서 암 조직의 내부와 주변에 퍼졌고, 72시간까지 강한 효과를 보였다.
연구팀은 CXCL10을 EASI로 투여한 이후 Th1(1형 도움 T세포) CD4 세포와 주효성 CD8 세포, NK세포 등의 종양 침윤이 증가한 걸 관찰할 수 있었다.
Th1 CD4 세포는 종양을 통제하는 데 도움이 되는 전 염증성 화학물질을 분비하고, NK세포는 암세포를 직접 살상한다.
실제로 적혈구를 이용하는 EASI로 이뮤노베이트를 전달하면, 폐 전이암 진행을 억제하는 효과가 그냥 CXCL1O을 투여했을 때보다 4배, 이뮤노베이트 형태로 투여했을 때보단 6배 강해졌다.
EASI 치료 후 37일이 지나자 생쥐 한 마리당 전이 혹(metastatic nodule)이 20개 이하로 줄었고, 단 한 개의 혹만 남은 생쥐도 25%에 달했다.
다른 치료법을 쓴 생쥐의 경우 적게는 2개, 많게는 100개의 혹이 남았다.
또한 EASI 치료를 받은 생쥐의 25%는 40일간 살아남았지만, 다른 치료를 받은 생쥐는 20일 안에 모두 죽었다.
EASI 치료를 받은 생쥐는 혈액의 기억 CD8 세포 수도 증가했다. 이 세포는 장기간 남아 있다가 면역성을 저해하는 위협이 다시 고개를 들면 경보를 울린다.
연구팀은 폐 전이암에 EASI 치료를 하면 전신에 종양 발달 억제 면역이 생긴다는 것도 확인했다.
논문의 교신저자인 미트라고트리 박사는 "우리 팀의 EASI 시스템을 쓰면 암 전이에 따른 생물학적 난관을, 독특한 전이암 치료 기회로 전환할 수 있다"고 말했다.
