실험 신약 페레솔리맙(peresolimab)이 류마티스 관절염의 새로운 치료제로 선택할만하다는 초기 임상시험 결과가 나왔다. 류마티스 관절염은 노인들에게 흔히 나타나는 퇴행성 관절염(골관절염)과는 달리 면역세포의 일종인 T세포가 팔목, 손가락, 발가락, 발목, 무릎 등 신체의 관절이 있는 부위를 공격해 발생하는 자가 면역 질환으로 모든 연령대에서 발생할 수 있다. 증상은 호전과 악화를 반복한다. 페레솔리맙은 류마티스 관절염 환자의 잘못된 면역체계를 올바른 상태로 되돌리는 효과가 있는 것으로 임상시험에서 밝혀졌다고 이 신약을 개발한 일라이 릴리(Eli Lilly) 제약회사가 발표했다고 헬스데이 뉴스(HealthDay News)가 최근 보도했다. 이 신약은 12주에 걸쳐 진행된 2a상 임상시험에서 관절 통증, 관절 부종, 압통, 염증을 크게 완화하는 효과가 있는 것으로 나타났다고 임상시험을 진행한 릴리 연구실의 면역 담당 부사장 아자이 니룰라 박사가 발표했다. 페레솔리맙은 면역체계에 제동을 거는 인간 세포 예정사 단백질-1(PD-1: human programmed cell death protein 1)을 자극하는 단클론 항체(monoclonal antibody)
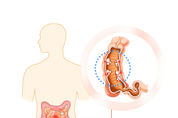
미국 식품의약청(FDA)은 표준 치료제가 잘 듣지 않는 크론병(Crohn's disease) 치료제로 경구용 우파다시티닙(제품명 린버크)을 승인했다. 크론병은 궤양성 대장염(UC: ulcerative colitis)과 함께 2대 염증성 장 질환(IBD: inflammatory bowl disease)의 하나로 소화기관 전체에서 발생할 수 있다. 대장과 소장이 연결되는 부위에서 발병하는 경우가 많고 그다음으로 대장, 회장 말단부, 소장 등에서 발생한다. 염증성 장 질환은 면역체계가 대장(궤양성 대장염) 또는 주로 소장(크론병)을 표적으로 오인, 공격함으로써 장 점막에 다발성 궤양과 출혈, 설사, 복통을 일으키는 만성 난치성 장 질환이다. 완화-재발이 반복하며 진행된다. FDA는 류마티스 관절염 등 다른 질환 치료제로 승인된 우파다시티닙을 종양괴사 인자(TNF·tumor necrosis factor) 차단제가 듣지 않는 중등도(moderate) 내지 중증 크론병 환자를 위해 쓸 수 있도록 적응증 추가를 승인했다고 헬스데이 뉴스(HealthDay News)가 최근 보도했다. 우파다시티닙은 애브비(AbbVie) 제약회사가 개발한 야누스 키나제(JAK·Janus ki
스타틴 계열(-statin) 계열의 고지혈증 치료제가 부정맥의 하나인 심방세동(AF: atrial fibrillation)으로 인한 뇌졸중과 '미니 뇌졸중'이라고 불리는 일과성 허혈 발작(TIA: transient ischemic attack) 위험을 막는 데 도움이 된다는 연구 결과가 나왔다. 심방세동은 심장의 윗부분인 심방이 이따금 매우 빠른 속도로 수축, 마치 그릇에 담긴 젤리처럼 가늘게 떠는 상태가 되면서 심박수가 분당 100회 이상으로 급상승하는 현상으로 방치하면 뇌졸중으로 이어질 수 있다. 홍콩 대학 의대의 황자이(Jiayi Huang) 교수 연구팀이 2010~2018년 사이에 심방세동 진단을 받은 5만1천472명의 의료기록을 분석한 결과 이 같은 사실이 밝혀졌다고 헬스데이 뉴스(HealthDay News)가 최근 보도했다. 이 중 1만1천866명은 평소 스타틴을 복용하고 있었고 나머지 3만9천606명은 스타틴을 사용하지 않았다. 연구팀은 두 그룹의 평균 5.1년 간 의료기록을 비교 분석했다. 그 결과 스타틴 그룹은 뇌경색과 전신성 색전증(systemic embolism) 발생률이 대조군보다 17% 낮은 것으로 나타났다고 연구팀은 밝혔다. 전신성

대웅바이오는 당뇨병 치료제 '베나보정'(성분명 이나보글리플로진)을 출시했다고 19일 밝혔다. 베나보는 신장에서 포도당의 재흡수에 관여하는 나트륨-포도당 공동수송체2(SGLT-2)를 억제해 소변으로 포도당을 배출하도록 하는 치료제다. 적응증(치료범위)은 단독요법, 메트포르민 병용요법, 메트포르민과 인슐린 분비 호르몬 분해효소(DPP-4) 억제제 병용요법의 3건이다. 대웅바이오 관계자는 "베나보 출시를 통해 당뇨병 치료 옵션을 늘려 환자의 삶의 질 개선에 기여할 것"이라고 말했다. 의약품 시장조사기관 유비스트에 따르면 지난해 2월 당뇨병 시장 규모는 1조5천억 원을 기록했으며 SGLT-2 억제제 계열 단일제와 복합제 처방액은 전년 대비 22% 증가한 1천826억 원으로 나타났다.

미국 식품의약청(FDA)은 주의력 결핍 과잉행동 장애(ADHD: attention-deficit/hyperactivity disorder) 치료제로 쓰이는 중추신경 자극제(각성제: stimulant)의 복약설명서 경고 내용을 한층 강화하도록 했다. FDA는 중추신경 자극제들이 남용되고 비의료용(non-medical)으로 오용되고 있는 데 대한 우려에서 이 같은 조치를 내렸다고 의학 뉴스 포털 메드페이지 투데이(MedPage Today)가 최근 보도했다. 중추신경 자극제에는 암페타민(제품명: 아데랄)과 메틸페니데이트(리탈린, 콘서타) 등이 있다. FDA는 모든 중추신경 자극제의 복약설명서에 강력한 수준의 경고인 '박스 경고'(boxed warning)를 넣고 오남용, 중독, 과다 복용, 사망 위험 등을 이해하기 쉬운 일반적인 언어로 자세히 설명하도록 했다. 예를 들어, 현재의 복약설명서에는 "남용과 의존 가능성"이 있다고 되어 있는데 이를 "경고: 남용, 오용, 중독" 가능성이 있다고 바꾸라는 것이다. 또 과다 복용하거나 코로 흡입하거나 주사하면 사망 위험이 있다는 경고문도 새로 넣도록 했다. 경고문에는 중추신경 자극제를 처방받은 뒤 과다 복용하거나 오남용하거

미국 일라이 릴리(Eli Lilly) 제약회사가 개발한 알츠하이머 치매 실험 신약 도나네맙(donanemab)이 초기 치매의 진행을 35% 억제하는 효과가 있는 것으로 밝혀졌다. 릴리 사는 3상 임상시험에서 이 같은 효과가 확인됐다면서 6월 말까지 미국 식품의약청(FDA)에 도나네맙을 정식 승인해 주도록 신청할 예정이라고 밝혔다고 AFP 통신과 헬스데이 뉴스(HealthDay News)가 최근 보도했다. 릴리 사의 최고 의학 책임자(CMO) 다니엘 스코브론스키 박사는 초기 알츠하이머 치매 환자 1천182명을 대상으로 18개월에 걸쳐 진행한 첫 번째 3상 임상시험에서 도나네맙이 투여된 실험군이 위약(placebo)이 투여된 대조군보다 치매 증상의 진행이 35% 느린 것으로 나타났다고 발표했다. 이는 '통합 알츠하이머병 평가 척도'(iADRS·Integrated Alzheimer's Disease Rating Scale)로 재정 관리, 운전, 취미 활동, 일상 대화 등 일상생활 수행 기능을 평가한 결과라고 그는 설명했다. 실험군에서는 47%(대조군은 29%)가 1년 후까지 증상이 진행되는 징후가 나타나지 않았다. 실험군에서는 52%가 1년 전에 투약을 중지할 수

식품의약품안전처는 최근 상분리 현상이 확인된 어린이 해열제인 '콜대원키즈펜시럽'을 제조한 대원제약에 사전예방적 차원에서 자발적 회수를 권고하고 제조·판매를 잠정적으로 중지하도록 조치했다고 18일 밝혔다. 식약처는 콜대원키즈펜시럽과 함께 대원제약이 수탁제조하는 다나젠의 '파인큐아세트펜시럽'에도 같은 처분을 내렸다. 이에 따라 대원제약과 다나젠은 사용기한이 남은 모든 제조번호 제품을 자발적으로 회수하기로 했다. 이들 제품과 동일하게 아세트아미노펜을 단일 주성분으로 하는 타사 액상시럽제와 현탁제에서는 상분리 현상이 확인되지 않았다고 식약처는 설명했다. 식약처는 온라인 커뮤니티 등에서 콜대원키즈펜시럽의 가루와 액체가 분리되는 상분리 현상이 나타난다는 정보를 인지하고 검토를 진행했다. 일부에선 한 포 전부가 아닌 일부를 복용하는 영아의 경우 상분리 현상이 발생하면 적정 용량보다 많은 약 성분이 투여될 수 있다고 우려했다. 점검 결과 두 제품의 제조공정과 품질관리 과정에서 위반사항은 발견되지 않았다. 또 전문가들은 현탁제 특성상 일부 성분이 가라앉아 상분리 현상이 발생할 수 있으며 이를 분할해 복용하는 경우에도 실제 위험성은 낮다는 의견을 냈다. 다만 상분리 제품을 분

구글 클라우드는 16일(현지시간) 신약 개발을 가속화하고 정밀 의학을 발전시키는 데 도움이 되는 두 가지 새로운 인공지능(AI) 기반 솔루션을 출시한다고 밝혔다. '타겟 및 리드 식별 제품군'(Target and Lead Identification Suite)이라는 이름의 한 솔루션은 신약 개발의 기본 요소인 단백질 구조를 예측하고 이해하는 데 도움이 되도록 설계됐다. 또 다른 도구인 '멀티오믹스 제품군'(Multiomics Suite)은 대량의 게놈 데이터를 수집해 저장하고 분석 및 공유할 수 있도록 도와준다. '멀티오믹스'는 유전체 등 분자 수준 데이터를 통합 분석하는 기술이다. 이 두 솔루션은 생명·바이오 업계의 숙원인 신약을 미국 시장에 출시하는 데 걸리는 시간과 비용을 크게 줄일 것으로 구글은 기대하고 있다. 글로벌 컨설팅업체 딜로이트가 최근 내놓은 보고서에 따르면 신약 하나를 출시하는 데 드는 비용은 최대 20억 달러 이상에 달한다. 엄청난 비용과 함께 10년에서 15년 동안 연구 과정도 수반된다. 막대한 자금을 투자해도 항상 성공하는 것은 아니며, 임상 시험까지 도달한 의약품 가운데 미국에서 승인받는 확률은 16%에 불과하다. 구글 클라우드의 생

미국 식품의약청(FDA)은 갱년기 장애 치료제로 개발된 페졸리네탄트(fezolinetant)를 비호르몬 계열의 경구용 안면홍조(hot flash) 치료제로 최초 승인했다. 안면홍조는 야한증(night sweat)과 함께 폐경 후 나타나는 혈관운동 증상(VMS: vasomotor symptom)으로 얼굴이 붉어지면서 화끈거리는 현상이다. 한 번 시작되면 짧게는 몇 초에서 길게는 1시간까지 계속되며 잦으면 하루에 20번까지 발생한다. 페졸리네탄트(제품명: 베오자)는 뉴로키닌-3 수용체 길항제(neurokinin-3 receptor antagonist)로 비호르몬 제제이다. FDA는 뇌의 체온 조절 기능을 돕는 이 약을 중등도(moderate) 내지 중증 안면홍조 치료제로 승인했다고 AP통신 등이 최근 보도했다. 페졸리네탄트는 45mg 짜리 캡슐을 매일 같은 시간에 복용하도록 되어있다. 페졸리네탄트는 12주 동안 진행된 3상 임상시험(SKYLIGHT-2)에서 안면홍조 발생을 하루 평균 7.5회 줄여주는 효과가 있는 것으로 나타났다. 40주 연장 임상시험에서는 안면홍조가 하루 평균 8.48회 감소하는 것으로 나타났다. 안면홍조 중증도(severity)도 크게 완화됐