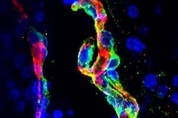
흔히 아테롬성 동맥경화라고 하는 죽상경화증(粥狀硬化症ㆍatherosclerosis)은 동맥 등 혈관 내피에 죽상경화반(atherosclerotic plaques)이 쌓여 혈관이 좁아지는 질환이다. 죽상경화반은 지방, 콜레스테롤, 칼슘 등의 혈액 성분이 뒤섞여 덩어리를 형성한 걸 말한다. 이런 죽상경화반이 동맥 내벽에 축적되면 산소가 포함된 혈액이 장기나 조직에 제대로 전달되지 못한다. 초기엔 별다른 증상이 없지만 나이가 들어 심해지면 관상동맥질환, 뇌졸중, 심근경색, 말초동맥질환 등으로 진행된다. 보통 65세쯤 되면 정도의 차이는 있어도 동맥경화가 있는 거로 간주한다. 선진국에서 동맥경화는 질병 사망 원인 1위로 꼽히는 위험한 병이다. 이런 죽상경화증의 예방과 치료에 큰 도움이 될 수 있는 뇌-혈관 신호 교환 메커니즘이 발견됐다. 동맥경화가 진행된 혈관의 전기 신호가 뇌로 전달되면 뇌가 스트레스 신호를 반송해 증세가 더 나빠진다는 게 요지다. 이 신호 회로를 끊으면 동맥경화의 진행이 억제된다는 것도 동물 실험에서 확인됐다. 독일 뮌헨대(LMUㆍ루트비히-막시밀리안 뮌헨대) 과학자들이 주도적으로 수행한 이 연구 결과는 지난달 27일(현지 시각) 저널 '네이처'(

밤에 잠을 못 자는 불면증(insomnia)과 낮에 각성 유지가 어려운 기면증(narcolepsy)은 마주 보는 거울처럼 정반대의 증상을 보인다. 하지만 불면증과 기면증의 뿌리는 같다. 히포크레틴(hypocretin)이라는 신경 펩타이드(neuropeptide)의 발현 수위에 따라 진행 방향이 달라질 뿐이다. 불면증에 시달리는 사람은 뇌(시상하부)에 히포크레틴이 너무 많고, 기면증 환자는 너무 적다. 히포크레틴은 우울증, ADHD(주의력 결핍 과잉행동 장애) 등의 정신 질환에도 관여하는 것으로 의심된다. 히포크레틴은 진작에 수면 장애 연구자들의 관심을 끌었다. 캐나다에선 2018년 히포크레틴의 작용을 억제하는 불면증 치료제가 도입됐다. 하지만 뇌 신경세포(뉴런)의 히포크레틴 수위가 어떻게 조절되는지에 대해선 지금까지 거의 알려진 게 없다. 이런 관련 지식의 부재는 히포크레틴을 표적으로 하는 치료제 개발에 큰 걸림돌이 됐다. 마침내 특정 유형의 마이크로 RNA(miR)가 인간의 히포크레틴 유전자를 표적으로 삼아 수면의 질과 양을 조절하는 메커니즘이 밝혀졌다. 마이크로 RNA가 수면 조절에 관여한다는 게 입증된 건 처음이다. 마이크로 RNA는 20∼25개의 뉴클
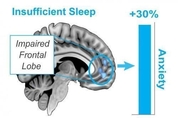
수면이 뇌의 인지 기능과 정신 건강에 중요하다는 건 익히 알려진 사실이다. 실제로 뇌에 쌓인 노폐물은 잠자는 동안, 특히 숙면할 때 제거된다. 그런데 나이가 들면 수면 패턴이 달라진다. 잠이 잘 오지 않거나 잠자다 깨는 경우가 잦아지면서 수면의 질과 양이 모두 떨어진다. 특히 고령자에게 이런 수면 장애가 오면 인지 기능 저하 등 신경정신 질환으로 이어질 위험도 커진다. 수면의 양이 너무 많은 것도 문제다. 특히 고령자는 수면 부족 못지않게 건강에 해롭다는 게 잇따라 보고되고 있다. 그럼 중년 이후 인지 기능 저하를 막고 정신 건강을 지키려면 하루 몇 시간의 수면이 적절할까. 영국과 중국 과학자들이 공동 연구를 통해 '하루 7시간'의 수면이 가장 이상적이라는 걸 밝혀냈다. 케임브리지대와 상하이 푸단대(復旦大學) 과학자들이 함께 수행한 이 연구 결과는 최근 저널 '네이처 노화'(Nature Aging)에 논문으로 실렸다. 연구팀은 '영국 바이오뱅크'(UK Biobank)에 등록된 38∼73세 성인 약 50만 명을 대상으로 수면 패턴, 정신 건강 상태, 삶의 질 등을 조사했다. 이 가운데 약 4만 명은 인지 기능 검사와 함께 뇌 영상 및 유전자 데이터도 분석했다.
면역계는 과거에 바이러스나 박테리아 같은 병원체와 만났던 걸 기억한다. 적응 면역계에서 주로 확인된 이런 '면역 기억'(immune memory)은 큰 자산이다. 동종 병원체가 다시 침입했을 때 면역 기억이 작동해야 신속하게 면역 반응을 일으킬 수 있다. 하지만 만성 염증 같은 내부 요인이 면역 기억을 자극하면 오히려 해로운 결과를 가져올 공산이 크다. 과민 면역 반응으로 자기 세포가 공격받는 자가면역질환이 대표적인 예다. 지금까지 과학자들은 선천 면역계의 면역 기억이 어떻게 작동하는지 잘 몰랐다. 그런데 선천 면역 기억이 염증을 촉발하면 다른 유형의 염증이 훨씬 더 심해진다는 흥미로운 연구 결과가 나왔다. 선천 면역 기억은 골수의 면역세포 전구체(immune cell precursor)에 후성 유전적 변화를 일으키는 것으로 밝혀졌다. 과학자들은 생쥐 모델 실험에서 잇몸 염증과 관절염 사이에 이런 메커니즘이 작용한다는 걸 입증했다. 잇몸 염증이 있는 생쥐의 골수를 건강한 생쥐에게 이식하면 더 심한 관절염이 생긴다는 것이다. 이 메커니즘은 다양한 '동반 질병'(comorbidity)의 연관성을 설명하는 근거가 될 수 있다. '동반 질병'은 병리학적으로 관련이
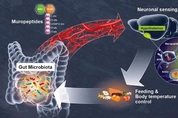
장(腸)의 미생물(gut microbiota) 세포에서 떨어진 부산물은 혈액을 타고 순환하면서 면역, 물질대사, 뇌 기능 등을 조절하는 거로 알려졌다. 장과 뇌 사이에 신호 전달 경로가 존재한다는 '장뇌 축'(gut-brain axis) 이론이다. 그런데 과학자들은 지금까지 이 이론을 입증할 만큼 명백한 근거를 제시하지 못했다. '장뇌 축'이 실제로 어떻게 작동하지도 설명할 수 없었다. 마침내 프랑스 과학자들이 뇌와 장 미생물 사이의 신호 교환 메커니즘을 밝혀냈다. 장 생태계에 변화가 생기면 뇌의 시상하부 뉴런이 곧바로 이를 감지해 식욕, 체온 등을 조절한다는 게 요지다. 비유하자면 뇌가 장 세균과 직접 의사를 소통한다는 뜻이다. 이 발견은 장차 비만, 당뇨 등의 대사 질환을 퇴치하는 획기적인 치료법 개발로 이어질 수 있다. 파스퇴르 연구소 과학자들이 주도한 이 연구엔 프랑스의 국립 보건의료연구소(Inserm)와 국립 과학연구원(CNRS) 과학자들도 참여했다. 관련 논문은 최근 저널 '사이언스'(Science)에 실렸다. 장은 인체 내에서 가장 큰 세균 저장소다. 한마디로 인간과 장 세균은 서로 의존하는 관계다. 장 세균은 숙주인 인간에 기생하면서 소화 작용
'면역 관문'(immune checkpoint)을 억제하는 항암제가 처음 등장했을 때 과학자들은 암 치료의 신기원을 열 거로 기대했다. 면역 관문 억제제는 암세포를 공격해 죽이는 '세포 독성 T세포'(cytotoxic T cells)가 면역 관문의 방해를 받지 않고 제 기능을 수행하게 하는 약이다. 하지만 지난 10여 년간 이 면역 항암제가 보인 치료 효능은 기대보다 낮은 것으로 평가된다. 사실 치료 효과를 실제로 본 환자보단 전혀 반응하지 않은 환자가 더 많다. 이런 유형의 면역 항암제가 아직 불완전하고 더 많은 연구가 필요하다는 지적도 제기되고 있다. 그러던 차에 기존 면역 관문 억제제의 결점을 획기적으로 보완할 수 있는 새로운 유형의 면역세포가 발견됐다. 이 면역세포는 기존 면역 항암제의 주 표적인 '세포 독성 T세포'보다 암세포 공격력이 훨씬 뛰어나다. 세포 독성 T세포(일명 킬러 T세포)와 달리 장기간 활동해도 탈진하지 않고, 더 깊은 조직에 숨어 있는 암 종양도 공격하는 것으로 확인됐다. 과학자들은 이 면역세포에 '타고난 킬러 같은 T세포'(killer innate-like T cell)라는 이름을 붙였다. 미국의 메모리얼 슬론 케터링 암센터(MS
전이암은 원발 암에서 떨어져나온 암세포 그룹이 다른 기관이나 조직으로 옮겨가는 걸 말한다. 원래 종양에서 이탈한 암세포 집단(cluster)은 먼저 주변의 미세환경에 침윤한다. 그런 다음 혈액과 림프 혈관을 타고 몸 안을 돌다가 멀리 떨어진 건강한 조직에 착근해 전이암을 형성한다. 이렇게 암이 전이하면 환자의 생존율이 뚝 떨어진다. 실제로 암 환자 사망의 절대다수는 전이암에서 발생한다. 지금까지 암이 어느 기관으로 전이할지는 부분적으로 원발 암 조직에 의존해 결정되는 거로 알려졌다. 전이성 유방암의 경우 주로 뼈로 옮겨가지만 간, 폐, 뇌 등에서 발견되기도 한다. 똑같이 유방 종양에서 이탈한 암세포 그룹이 어떻게 어느 기관으로 전이할지 결정할까. 스위스 제네바대(UNIGE) 의대와 취리히 연방 공대(ETHZ) 과학자들이 유방암 세포의 전이 부위 결정 메커니즘을 밝혀냈다. 암세포가 주변 환경에 맞춰 기능과 형태를 바꾸는 적응 능력(plasticity)이 전이 기관을 결정하는 핵심 요인이었다. 과학자들은 이 과정에 깊숙이 개입해 암세포의 적응 능력을 제어하는 단백질도 발견했다. 이 연구 결과는 저널 '네이처 커뮤니케이션'(Nature Communications)
매우 위험한 암으로 꼽히는 췌장암의 5년 생존율은 약 10%에 불과하다. 고지방식을 많이 섭취하는 미국에서 췌장암은 암 사망 원인 3위에 올라 있다. 췌장암 치료가 이렇게 어려운 이유는 망(網) 구조의 섬유질 조직이 종양을 둘러싸고 있기 때문이다. 이 섬유질 망은 치료제의 접근을 막아 결과적으로 종양의 공격적인 성장을 촉진한다. 마침내 미국 뉴욕대(NYU) 과학자들이 췌장암의 섬유질 망이 생기는 메커니즘을 밝혀냈다. 핵심 역할을 하는 건 면역세포의 일종으로 병원체와 노폐물 등을 집어삼키는 대식세포(macrophage)였다. 이 연구는 미국 뉴욕 소재 학술 의료 센터인 'NYU 랑곤 헬스'(NYU Langone Health)의 다프나 바 사기(Dafna Bar-Sagi) 생화학 분자약리학 교수팀이 수행했다. 관련 논문은 4일(현지 시각) 미국 국립과학원회보(PNAS)에 실렸다. 바 사기 교수팀은 이전의 연구를 통해 대식세포가 췌장암 종양을 격리하는 콜라젠에 특이하게 작용한다는 걸 알고 있었다. 종양 주변에 콜라겐이 너무 많이 쌓이면 비정상적 변환을 거쳐 섬유조직이 형성되는데 대식세포가 이 과정에 깊숙이 관여했다. 이런 환경에서 대식세포는 마노스 수용체(MRC1
신종 코로나바이러스(SARS-CoV-2)의 오미크론 변이는 기존 변이보다 전염력이 강하지만, 감염 증상은 심하지 않다. 실제로 오미크론 변이에 감염돼도 대부분 감기 정도의 가벼운 증상 또는 독감과 비슷한 중등도 증상에 그치고 상당수는 무증상으로 모른 채 지나간다. 그렇다고 오미크론 변이로 사망하는 환자가 없는 건 아니다. 전파 속도가 아주 빠른 오미크론 변이는 폐 조직 깊숙이 퍼져 심각한 감염증을 일으키기도 한다. 미국에선 오미크론 감염으로 사망한 환자가 올해 들어서만 수천 명에 달했다. 그런데 오미크론 변이가 우세 종으로 자리를 잡으면서 특이한 현상이 과학자들의 눈에 포착됐다. 알레르기성 천식 환자가 유난히 오미크론 감염에 강하다는 것이다. 이런 유형의 천식 환자는 중증 코로나19(신종 코로나바이러스 감염증)로 진행되는 경우가 훨씬 적다. 비슷한 만성 질환인 COPD(만성 폐쇄성 호흡기 질환)나 폐 기종 환자는 중증 코로나19 위험이 매우 크다. 미국 노스캐롤라이나대(UNC) 의대 과학자들이 이런 차이가 생기는 이유를 밝혀냈다. 염증성 사이토카인(면역 단백질)인 인터류킨-13(IL-13)이 핵심 역할을 했다. IL-13은 숙주세포의 ACE2 발현 등을 제어