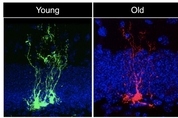
실제 나이와 생물학적 노화(biological aging)는 일치하지 않는 경우가 많다. 실제로 외모가 나이보다 젊게 보이는 사람도 있지만 더 늙어 보이는 사람도 적지 않다. 나이가 들면 뇌세포도 퇴행하는데 여기에 깊숙이 관여하는 게 신경줄기세포((NSCs)다. 신경줄기세포는 여러 가지 신경세포로 분화할 수 있는 만능 세포를 말한다. 배아 발생 과정에서 신경줄기세포는 신경 전구세포를 만들고, 신경 전구세포는 신경세포나 교세포가 된다. 신경줄기세포는 특히 나이가 들면서 찾아오는 노화에 취약하다. 기본적인 인지 기능의 퇴화는 물론이고 치매, 알츠하이머병, 간질, 뇌 손상 등의 신경질환도 신경줄기세포의 노화와 관련이 있다. 이런 신경줄기세포의 노화가 어떻게 일어나는지를 미국 서던캘리포니아대(USC) 과학자들이 밝혀냈다. 신경줄기세포의 노화를 촉진하는 유전자 네트워크와 그 안에서 일종의 허브(hub) 역할을 하는 핵심 유전자(Abl 1) 유전자를 찾아낸 것이다. 연구팀은 또 백혈병 치료제로 미국 FDA(식품의약국) 승인을 받은 글리벡(일반명 이매티닙)이 Abl 1 유전자의 발현을 억제한다는 것도 동물실험에서 확인했다. USC 의대의 마이클 보나구이디 교수 연구팀이
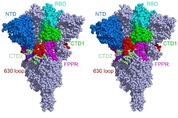
뉴클레오캡시드(Nucleocapsid)는 바이러스의 유전체(genome)를 감싸서 보호하는 핵산단백질을 말한다. 항체 결합 사이트를 비롯한 유사한 구조의 핵산단백질이 많은 코로나 계열 바이러스에 보존돼 있다는 걸 미국 펜실베이니아 주립대(Penn State) 과학자들이 발견했다. 여기엔 신종 코로나는 물론이고 최근 잇따라 출현한 신종 코로나 변이도 포함된다. 연구팀은 또 코로나19(신종 코로나바이러스 감염증) 환자의 항체가 이 단백질과 어떻게 결합하는지도 확인했다. 이 발견은 특히 대유행 위험 요인으로 급부상한 신종 코로나 변이와 관련해 주목된다. 신종 코로나의 핵산단백질이 스파이크 단백질을 대체할 이상적인 치료 표적이 될 수 있기 때문이다. 연구 결과는 최근 영국 왕립화학협회가 발간하는 저널 '나노스케일'(Nanoscale)에 논문으로 실렸다. 12일 미국 과학진흥협회(AAAS) 사이트(www.eurekalert.org)에 공개된 논문 개요 등에 따르면 연구팀은 코로나 계열 바이러스의 전체 핵산단백질 구조를 이번에 처음 밝혀냈다. 연구를 이끈 뎁 켈리 분자 생물물리학 석좌 교수는 "사스 바이러스(SARS-CoV-1)부터 변이한 신종 코로나까지 (비슷한 구조
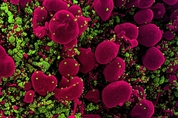
신종 코로나바이러스(SARS-CoV-2)와 감기 바이러스(common-cold virus)는 모두, 왕관 모양의 스파이크 단백질 돌기를 가진 코로나 계열 바이러스다. 스파이크 단백질은 코로나바이러스가 인체 세포에 감염할 때 꼭 필요하다. 스파이크 단백질이 인체 세포와 결합해 '막(膜) 융합'을 일으켜야 바이러스 입자가 세포 안으로 들어가는 침투로가 열린다. 그런데 시간이 지나 스파이크 단백질에 돌연변이가 축적된 감기 바이러스는 혈장 항체의 중화 작용을 회피하는 것으로 밝혀졌다. 이 발견은 인간의 면역계가 신종 코로나바이러스의 진화 유형을 결정하는 데 중요한 역할을 한다는 가설을 뒷받침한다. 아울러 신종 코로나바이러스가 지금처럼 변이를 거듭하면 기존 백신의 효과가 크게 떨어질 수 있음을 시사한다. 미국 프레드 허친슨 암 센터 과학자들이 수행한 이 연구 결과는 8일(현지 시각) 저널 'PLOS 패소전스'(PLOS Pathogens)에 논문으로 실렸다. 사실 코로나 계열 바이러스는 알려진 것만 수백 종에 달한다. 다행히 인간에게 감염해 질병을 일으키는 건 현재 대유행 중인 신종 코로나와 사스(중증 급성호흡기증후군) 코로나(SARS-CoV), 메르스(중동호흡기증후군
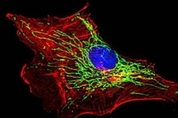
세포가 스트레스를 받으면 화학적 경보가 발령돼 '세포 발전소' 미토콘드리아를 지키는 일련의 생리 현상이 벌어진다. 이 과정에서 앞장서 미토콘드리아의 건강을 보호하는 게 파킨(Parkin) 단백질이다. 손 떨림, 경직, 불안정한 자세 등 운동 이상을 특징으로 하는 파킨슨병에는 산발형과 가족형(familial Parkinson's disease) 두 종류가 있는데 가족형은 파킨 단백질의 유전자 돌연변이와 관련이 있는 것으로 알려졌다. 이 파킨 단백질이 세포 스트레스를 감지하는 '마스터 센서'와 곧바로 연결돼 있다는 걸 미국 소크 연구소 과학자들이 발견했다. 특히 주목할 만한 부분은 이 분자 경로가 암이나 2형 당뇨병의 발생 과정에도 관여한다는 것이다. 이 연구 결과가 이들 3가지 질병의 치료법 개발에 새로운 길을 열 수 있다고 과학자들은 말한다. 소크 암 센터의 루벤 쇼 교수 연구팀은 7일(현지 시각) 저널 '사이언스 어드밴시스'(Science Advances)에 관련 논문을 발표했다. 이 센터의 소장인 쇼 교수는 이번 연구 논문의 수석저자도 맡았다. 파킨 단백질의 주 기능은 세포 스트레스로 손상된 미토콘드리아를 제거해 건강한 미토콘드리아가 보충되게 하는 것이다
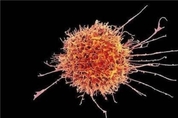
'핵 얼룩(nuclear speckles)'은 포유류의 세포핵 내에 존재하는 '이어 맞추기 인자(splicing factor)' 항체로, RNA 합성이 중지되면 둥근 형태로 응집하는 성질이 있다. 전자현미경으로 보면 대체로 균일한 입자 덩어리(IGC)와 크로마틴(염색질) 주변 섬유로 구성돼 있다. 처음 발견된 건 1910년으로 111년이 지났지만, 핵 얼룩이 어떤 기능을 하는지는 별로 알려진 게 없다. 신비의 베일에 싸였던 이 세포핵 소체가, 암 억제 단백질 p53의 특정 유전자 그룹 조절에 핵심 역할을 하는 것으로 밝혀졌다. 이 발견은 암에 대한 이해 증진을 넘어서 획기적인 암 치료법 개발로 이어질 수 있다고 과학자들은 말한다. 미국 펜실베이니아 의대의 셸리 버거 세포·발달 생물학 교수 연구팀은 5일(현지 시각) 국제학술지 '몰레큘라 셀(Molecular Cell)'에 관련 논문을 발표했다. 논문의 수석저자를 맡은 버거 교수는 "핵 얼룩이 유전자 발현의 핵심 조절자 역할을 한다는 게 확인됐다"라면서 "이는 암에 대해서도 어떤 역할을 한다는 걸 시사한다"라고 말했다. 핵 얼룩엔 유전자의 DNA를 전사해 단백질 생성 정보를 가진 '전령 RNA'로 만드는 데 필
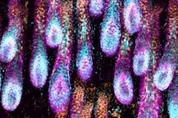
스트레스를 많이 받으면 탈모가 온다는 속설이 과학 실험을 통해 사실로 입증됐다. 만성 스트레스가 모낭(hair follicle) 줄기세포의 재생 기능을 방해하는 생물학적 메커니즘을 미국 하버드대 연구진이 밝혀냈다. 스트레스를 받을 때 분비되는 호르몬이, 모낭 줄기세포의 휴지기(rest phase)를 연장해 재생을 장기간 멈추게 하는 것으로 나타났다. 과학자들은 스트레스 신호가 모낭 줄기세포에 전달되는 분자 경로도 찾아냈다. 이 경로는 탈모 상태에서 머리가 다시 자라게 하는 치료 표적이 될 수 있다고 과학자들은 말한다. 이 연구 결과는 31일(현지 시각) 저널 '네이처'(Nature)에 실렸다. 논문의 수석저자인 수야츠에(Ya-Chieh Hsu) 줄기세포 재생 생물학과 부교수는 "스트레스가 모낭 줄기세포의 활성화를 늦추고, 조직 재생 주기에도 근본적인 변화를 가져온다는 걸 확인했다"라고 말했다. 모낭은 평생 재생 과정을 반복할 수 있는, 포유류의 몇 안 되는 조직 중 하나다. 모낭은 성장과 휴지(休止)의 사이클을 되풀이한다. 모낭 줄기세포가 활성화해 모낭과 모발을 재생하는 성장기엔 머리가 매일 자라지만, 줄기세포가 활동을 멈추고 쉬는 휴지기엔 머리가 쉽게 빠진
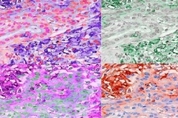
암 환자의 면역계를 이용해 암을 공격하는 면역치료는 처음 나왔을 때부터 새로운 길을 여는 획기적 치료법으로 주목받았다. 하지만 실제로 써 보니 치료비가 많이 들고 부작용이 심한데다 일부 환자에게만 치료 효과가 나타나는 한계를 드러냈다. 미국 시카고대 과학자들이 이런 단점을 대부분 보완한 항암 면역치료 백신을 개발해 동물 실험 에서 뚜렷한 효능을 확인했다. 이 백신은 환자 자신의 암세포를 표지 항원으로 이용해 면역계가 암 종양을 찾아 죽이게 하는 것이다. 이 백신을 생쥐 모델에 주사하면 흑색종의 성장이 멈췄고, 오랜 시간이 흐른 뒤에 신생 종양을 파괴하는 효과도 보였다. 시카고대의 프리츠커 분자 공대(Pritzker School of Molecular Engineering) 과학자들은 24일(현지 시각) 저널 '사이언스 어드밴시스'(Science Advances)에 관련 논문을 발표했다. 연구를 이끈 멜로디 스워츠 교수는 "효과가 더 좋고 훨씬 더 안전하면서 비용은 덜 드는 면역치료 전략"이라면서 "다른 항암 면역치료에서 생기는 문제도 대부분 극복할 수 있는, 진정한 개인 맞춤형 치료법"이라고 자평했다. 이 항암 백신의 작용 원리는 기존의 인플루엔자(독감) 백
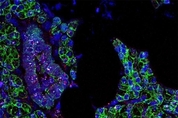
코로나19(신종 코로나바이러스 감염증) 환자의 침(唾液)엔 높은 수치의 신종 코로나 입자가 들어 있다. 타액으로 코로나19 감염 여부를 검사한다고 해도, 코안에 면봉을 깊숙이 넣어 검체를 채취하는 현재의 검사법보다 신뢰도가 떨어지지 않을 거라는 연구 결과도 나왔다. 지금까지 확실히 밝혀지지 않은 건, 몸 안의 어떤 부위로부터 침으로 옮겨왔느냐 하는 것이다. 예컨대 호흡기 증상이 있는 코로나19 환자의 경우 콧물이나 가래를 통해 바이러스가 침으로 퍼질 수 있다. 하지만 호흡기 증상이 거의 없는 코로나19 환자의 타액에서도 신종 코로나는 나온다. 마침내 이 의문점을 풀 수 있는 연구 결과가 나왔다. 신종 코로나가 입안 세포에 직접 감염한다는 사실을 미국 연구진이 밝혀냈다. 미국 국립보건원(NIH)과 노스캐롤라이나 치과대 등의 과학자가 공동 수행한 이 연구 결과는 25일(현지 시각) 저널 '네이처 메디신(Nature Medicine)' 온라인판에 논문으로 실렸다. 신종 코로나의 주 감염 표적은 폐와 상기도(upper airways)이지만, 소화계·혈관·신장 등에도 감염할 수 있다. 이번 연구 결과는 신종 코로나가 몸 안에 퍼지는 과정에서 입이 생각보다 중요한 역할
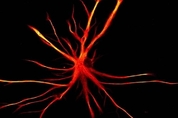
인간은 삶의 3분의 1을 잠자는 데 할애하면서도 수면이 어떤 기능을 하는지 잘 모른다. 예를 들면 어떤 이는 수면을 방해하는 환경에서도 깊게 잠들지만, 어떤 이는 밤마다 몇 시간씩 뒤척이며 잠을 설친다. 사람마다 피로가 풀렸다고 느끼는 수면량이 다른 이유도 우리는 알지 못한다. 그런데 뇌에서 흔히 발견되는 성상교세포(astrocytes)가 수면의 양과 질을 제어하는 데 중요한 역할을 하는 것으로 밝혀졌다. 과학자들은 성상교세포의 특정 수용체가 이런 수면 조절에 관여한다는 걸 확인했다. 별처럼 보인다고 해서 이런 이름이 붙은 성상교세포는 원래 뉴런(신경세포)에 대한 영양 공급 및 이온 농도 조절, 노폐물 제거 등을 하는 거로 알려졌지만 최근엔 뇌 신경회로를 직접 제어한다 는 연구 결과도 나왔다. 이번 연구를 수행한 미국 샌프란시스코 캘리포니아대(UCSF) 연구진은 최근 저널 '이라이프'(eLife)에 관련 논문을 발표했다. 23일 미국 과학진흥협회(AAAS) 사이트(www.eurekalert.org)에 공개된 논문 개요 등에 따르면 뇌의 성상교세포를 조작해 수면의 양과 질에 영향을 미친다는 걸 입증한 건 처음이다. 기본적으로 성상교세포는 뇌의 뉴런을 지지하는