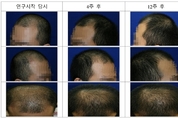
막이 없는 무(無) 막 줄기세포로 남성형 탈모증을 개선할 수 있다는 시험결과가 나와 눈길을 끈다. 양산부산대학교병원 이상엽 가정의학과 교수팀은 안드로젠 탈모증(남성형 탈모) 질환자를 대상으로 '무(無) 막 줄기세포 효과' 검증을 했다고 20일 밝혔다. 이 결과 탈모증 질환자의 모발 수가 3.6배 증가하고 모발 두께가 2.55배 굵어진 것을 확인했다. 이 교수팀은 이번 시험에서 양산부산대학교병원 기능성 식품연구소와 함께 줄기세포 연구기업인 '티스템'이 보유한 특허 기술로 생성한 무 막 줄기세포 추출물이 남성형 탈모에 얼마나 효과적인지 분석했다. 무 막 줄기세포는 면역 거부반응을 일으키는 세포막을 제거해 누구든지 사용할 수 있도록 만든 줄기세포를 일컫는다고 이 교수팀은 설명했다. 이번 시험은 만 18∼59세 남성형 탈모 남녀 38명을 무작위로 19명씩 두 그룹으로 나눠 진행됐다. 시험집단에는 시험물질인 무 막 줄기세포 추출물을 토닉 형태로 두피에 뿌렸고, 대조집단은 시험물질을 뿌리지 않아 외부 변인을 최소화했다. 연구 결과 시험집단 모발 수는 16주 차에 26% 증가했다. 대조집단은 같은 기간 자연 증가 수치에 해당하는 7.1% 증가에 그쳤다. 모발 두께는 16
차세대융합기술연구원(융기원) 정밀의학연구센터 공동연구팀은 항암 유전자 'p53'이 어떤 과정을 거쳐 암의 전이와 악성화를 촉진하는지 동물실험을 통해 규명했다고 20일 밝혔다. 그동안 p53 유전자의 손실이 암의 전이와 악성화에 기여한다는 추측만이 있었으나 이번 공동연구를 통해 이 현상과 원리를 명확히 증명했다. 융기원 정밀의학연구센터와 융기원에 입주한 벤처기업 테라젠바이오, 일본 가나자와대학 암연구소 공동연구팀은 동물실험을 통해 p53 유전자 변이와 손실이 암의 전이 병변에서 빈번하게 발생한다는 것을 관찰했으며 이들의 복합기능도 증명했다고 설명했다. 이번 p53 유전자 연구는 암의 전이를 억제하는 전략을 개발하는 데 도움이 될 것으로 연구팀은 기대했다 이번 연구 성과는 국제 학술지 '네이처 커뮤니케이션즈' 최신 호에 실렸다.
심장의 우심실 비대(right ventricle enlargement)가 신종 코로나바이러스 감염(코로나19) 중환자의 사망 위험을 예고하는 지표가 될 수 있다는 연구 결과가 나왔다. 우심실은 온몸을 돌면서 노폐물인 이산화탄소를 거둬들인 정맥혈을 우심방으로부터 받아 폐로 보내는 곳이다. 정맥혈은 폐에서 이산화탄소를 방출하고 산소를 새로 공급받은 뒤 다시 좌심방-좌심실을 거쳐 온몸으로 나간다. 미국 마운트 시나이 병원 심혈관 전문의 에드가 아걸리언 박사 연구팀은 코로나19 환자의 사망 위험과 크게 연관이 있는 유일한 변수는 우심실 비대라는 연구 결과를 발표했다고 CNN 뉴스 인터넷판이 19일 보도했다. 3월 26일부터 4월 22일 사이에 마운트 시나이 병원에 입원한 코로나19 환자 102명의 의료기록을 분석한 결과 이 같은 사실이 밝혀졌다는 것이다. 이 중 32명(31%)은 심장 초음파(echocardiogram) 검사에서 우심실 확대 판정을 받았고 그중 41%가 사망했다. 우심실 비대가 없는 다른 환자들은 11%가 사망했다. 이는 우심실의 변형(strain)이 코로나19 입원 환자의 불리한 결과와 연관이 있음을 보여주는 중요한 증거라고 연구팀은 설명했다. 따

부모의 형제자매 중에 자폐스펙트럼장애(ASD: 자폐증) 환자가 있어도 자폐증 위험이 높아진다는 연구 결과가 나왔다. 미국 워싱턴대학 아동병원 정신의학 실장 존 콘스탄티노 박사 연구팀이 스웨덴에서 2003~2012년 사이에 태어난 아동과 그 가족 약 85만명의 의료기록을 분석한 결과 이 같은 사실이 밝혀졌다고 메디컬 익스프레스(MedicalXpress)가 19일 보도했다. 부모의 형제자매 중 자폐증 환자가 있는 아이는 자폐증 진단율이 3~5%로 다른 일반 아이들의 1.5%보다 2~3배 높은 것으로 나타났다고 연구팀은 밝혔다. 어머니의 형제자매 중 자폐증 환자가 1~2명 있는 아이는 일반 아이들보다 자폐증 위험이 3배, 아버지의 형제자매 중 자폐증 환자가 1~2명 있는 아이는 2배 높은 것으로 나타났다. 이는 여성에게는 자폐증을 막는 방어 메커니즘이 있을 수 있다는 일반적인 이론에 의문을 제기하는 것일 수 있다. 자폐증 진단 비율은 남아가 여아보다 4대1로 훨씬 높은 것으로 알려져 있다. 이에 대해 미국 국립 아동건강·인간발달연구소(NICHD)의 앨리스 카우 박사는 남성이 자폐증 유병률이 높은 이유가 여성의 보호 효과 때문이 아님을 보여주는 것이라고 논평했다.
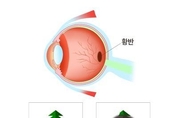
노인 실명 1위의 안과 질환인 노인성 황반변성(AMD: age-related macular degeneration)의 원인은 의외로 면역세포가 만드는 단백질 중 하나인 인터류킨-4(IL-4)일 수 있다는 연구 결과가 나왔다. 황반변성은 망막의 중심부에 있는 시신경 조직인 황반에 비정상적인 신생 혈관이 자라면서 황반이 손상돼 시야의 중심부를 보는 시력인 중심시(central vision)를 잃는 안과 질환이다. 일본 돗토리(鳥取) 대학 의학부의 안과 전문의 미야자키 다이 교수 연구팀은 습성(wet) 황반변성 환자의 눈 속 체액인 방수(房水, aqueous humor)에는 IL-4가 지나치게 많이 들어있으며 이것이 습성 황반변성의 원인일 수 있다는 연구 결과를 발표했다고 메디컬 뉴스 투데이가 17일 보도했다. 연구팀은 습성 황반변성 환자 234명과 백내장 노인 환자 104명을 대상으로 방수의 IL-4 수치를 측정했다. 그 결과 황반변성 환자가 대조군보다 IL-4 수치가 높았다. 원래 IL-4는 염증과 신생 혈관의 형성을 억제하고 신경세포를 보호하는 것으로 알려져 있다. 연구팀은 이것이 어떤 의미를 갖는 것인지 황반변성 모델 쥐를 대상으로 연구를 진행했다. 황반변
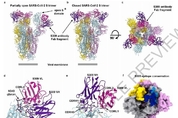
미국·스위스·프랑스 공동 연구진이 사스(SARS·중증급성호흡기증후군) 완치자로부터 분리한 항체를 이용해 코로나19 바이러스(SARS-CoV-2) 감염을 억제하는 실험에 성공했다. 미국 워싱턴대 생화학과 데이비드 비슬러 교수가 이끄는 연구팀은 18일(미국 현지시간) 과학저널 '네이처'(Nature)에서 2003년 사스에서 완치된 사람에게서 분리한 항체가 코로나19 바이러스 감염을 효과적으로 차단할 수 있음을 확인했다고 밝혔다. 항체는 인체에 침투하는 바이러스나 세균 등 외부물질에 대항하기 위해 면역체계가 만드는 것으로, 바이러스를 무력화할 수 있는 항체는 항바이러스 치료제나 백신 개발에 활용될 수 있다. 이 연구팀은 앞서 2003년 사스에서 회복된 한 환자로부터 SARS 코로나바이러스가 사람과 동물에 감염되는 것을 억제하는 단일클론항체를 분리해낸 바 있다. 단일클론항체는 병원체의 특정 단백질(항원) 하나를 표적으로 하는 항체로, 코로나19 바이러스가 인체 세포에 침투할 때 사용하는 돌기 단백질(spike protein)과 결합하는 단일클론항체를 찾으면 코로나19 치료 또는 감염예방에 이용할 수 있다. 연구팀은 이번 연구에서 이전에 분리해낸 항체 25개 가운데
최상위 질병 사망 원인으로 꼽히는 '주요 혈관성 이벤트'(major vascular events), 감염증, 암 등의 관련 질병 오진율이 미국에서 거의 10%에 육박한다는 연구 결과가 나왔다. 미국 기반의 연구 보고서와 문헌 기초 추정치 등을 분석해 산출한 결과다. 연구진은 이를 토대로 상위 3개 범주에서 각각 오진이 잦은 5개(도합 15개)의 질환을 가려내, 진단 실수에 따른 심각한 오진 피해 추정치를 계산했다. 여기서 심각한 오진 피해란, 영구적 기능 상실이나 사망으로 이어진 경우를 말한다. 상위 3개 범주의 15개 질환은, 전체 심각한 오진 피해의 53.9%를 차지했다. 이 연구를 주도적으로 수행한 미국 존스 홉킨스 의대의 데이비스 뉴먼-토커 신경학 교수팀은 17일 저널 '진단(Diagnosis)'에 관련 논문을 발표했다. 저널 '진단'은, 독일 '발터 데 그루이터' 출판사가 발행하는 의학진단개선협회(SIDM)의 공식 학술지다. 분석 결과 가장 희소한 감염증과 주요 혈관성 이벤트의 관련 질환에서 오진율이 가장 높았다. 상위 그룹의 15개 질환 중에는, 척수를 압박해 사지 마비를 일으키는 '척수 농양(spinal abscesses)'이 62.1%로 가장
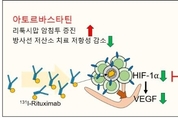
한국원자력의학원은 고지혈증 약인 아토르바스타틴을 방사면역치료제(방사성요오드-리툭시맙)와 함께 투여하면 저산소증으로 인한 암치료 저항성을 억제해 치료효과를 30% 이상 높일 수 있음을 동물실험으로 확인했다고 18일 밝혔다. 연구팀은 림프종 모델 쥐를 국내 고유기술로 제작한 방사면역치료제인 방사성요오드-리툭시맙 단독투여군, 방사성요오드-리툭시맙+아토르바스타틴 병용투여군으로 나눠 단일광자단층촬영(SPECT)으로 치료효과를 비교 관찰했다. 암세포는 증식과정에서 쉽게 저산소증 상태가 되고, 저산소증 암세포는 산소가 부족한 환경에서 살아남아 악성도가 증가, 방사선 치료를 어렵게 하는 요인이 된다. 방사면역치료는 방사선치료 효과와 표적항체의 면역작용 효과를 결합한 치료로 표적항체를 이용해 암세포에만 방사선을 조사, 정상세포에 미치는 방사선 영향은 최소화하고 암 치료 효과는 높인다. 아토르바스타틴을 병용 투여한 쥐는 종양에 침투되는 방사성 요오드-리툭시맙이 단독투여군보다 20% 이상 증가했고, 종양 살상 효과도 단독투여 때 보다 30% 이상 증가했다. 연구팀은 아토르바스타틴을 투여하면 산소가 부족한 환경에서 암세포가 적응할 수 있도록 하는 저산소증 유도인자 유전자(HIF-

인체 면역계가 신종 코로나바이러스(SARS-CoV-2)에 실질적이고 지속적인 면역 반응을 일으키는지는 아직 확실히 규명되지 않았다. 실제로 신종 코로나바이러스 감염증(코로나19)에 걸렸다가 회복돼도 면역력이 생기지 않는다는 우려가 의료계 안팎에 퍼져 있다. 특히 완치 판정을 받고 격리에서 풀려났다가 재감염되는 사례가 속출하면서 그런 회의론이 거세지는 것도 사실이다. 그런데 대표적인 면역세포인 T세포가 신종 코로나바이러스의 스파이크 단백질 등에 안정적인 면역 반응을 보인다는 완치자 테스트 결과가 나와 주목된다. 신종 코로나바이러스는 스파이크 단백질로 세포 표면의 ACE2 수용체와 결합해야 세포 안으로 들어간다. 그래서 스파이크 단백질은 코로나19 백신 개발의 주 표적으로 부상했다. 이번 연구 결과는 코로나19 완치자 시험에서 확보된 최초의 세포 면역 데이터로서, 향후 백신 개발 연구와 사회적 거리 두기 정책 등에 큰 도움이 될 거로 기대된다. 미국 라호야 면역학연구소 과학자들은 이런 내용의 논문을 16일 저널 '셀(Cell)'에 발표했다. 연구팀은 코로나19에 걸렸다가 회복한 완치자 20명의 혈액 샘플을 이용해 T세포 반응을 검사했다. 피험자 그룹은, 감염증의