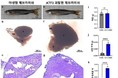
![생쥐 성상교세포의 액틴 세포 골격(적색)과 리소좀(녹색)<br>
[독일 FMP 제공 / 재판매 및 DB 금지]](http://www.hmj2k.com/data/photos/20200627/art_15935151752094_e11697.jpg)
우리 몸의 세포는 자가포식(autophagy)과 리소좀(lysosome) 용해를 축으로 하는 세포 노폐물 제거 시스템을 갖고 있다.
세포 기능에 문제를 일으키는 잘못 접힌 단백질이나 손상된 세포 소기관 등을 용해하고, 그 과정에서 생기는 아미노산 등의 부산물을 대사체계로 다시 투입하는 일종의 '쓰레기 재활용' 시스템이다.
이 시스템은 기본적으로 세포를 젊게 유지하는 작용을 하는 것으로 여겨진다. 예를 들면 알츠하이머병 같은 신경퇴행 질환에서 단백질의 이상 응집을 막는 것 같은 일이다.
그런데 세포의 수분이 빠지면서 형성되는 '삼투 압박(osmotic stress)'이 세포 노폐물 제거 시스템을 작동하는 핵심 기제라는 걸 독일 과학자들이 발견했다.
세포 내에서 물과 이온의 평형이 깨지면 몇 시간 안에 자가 포식소체(autophagosome)와 리소좀 수가 급증하고 활성도도 대폭 높아진다는 것이다.
이 연구는 라이프니츠 과학협회(Leibniz Association) 산하 분자약물학연구소(FMP) 과학자들이 수행했다. 관련 논문은 최근 저널 '네이처 세포 생물학(Nature Cell Biology)'에 실렸다.
자가포식과 리소좀 용해가 노화와 신경퇴행 질환에 핵심 역할을 한다는 건 많은 선행연구에서 보고됐다.
금식하면 세포 노폐물 제거 시스템이 작동하기 시작한다는 것에도 과학자들은 대체로 동의한다.
하지만 구체적으로 이 시스템을 움직이는 요인이 무엇인지는 지금까지 거의 밝혀지지 않았다.
과학자들은 성상교세포를 이용해 탈수 상태의 세포에서 어떤 일이 벌어지는지 관찰했다. 성상교세포는 뇌에서 신경세포(뉴런)의 기능을 돕는 면역세포다.
세포에서 수분이 빠지면 세포 안에 있던 NHE7 단백질(이온 운반체)이 외부와의 경계선인 원형질막으로 위치를 옮겼다.
그러면 나트륨 이온이 운반체를 타고 세포 내로 들어와 세포액의 칼슘 수위를 올렸다. 이어 칼슘 수위 상승은 TFEB라는 전사인자를 활성화했고, TTFEB의 활성화는 자가포식 유전자와 리소좀 유전자의 스위치를 올리는 연쇄반응이 일어났다.
간단히 말해 삼투 압박이 NHE7 이온 수송체를 자극한 게 전체 시스템 경로에 시동을 건 셈이다.
논문의 제1 저자인 타니아 로페츠-헤르난데츠 박사후연구원은 "특히 신경퇴행 질환은 이 경로가 바르지 않게 켜진 결과일 수 있다"라면서 "아울러 NHE7은 알츠하이머병의 위험 유전자이기도 한데 그 의미를 이해하는 통찰을 갖게 됐다"라고 말했다.