장(腸)의 미생물 중에는 건강에 이로운 종도 있지만, 질병을 일으키는 것도 없지 않다. 장 세균이 관여하는 병은 자가면역 질환, 염증성 장 질환, 대사 증후군, 신경정신 질환 등 의외로 많다. 이른바 '새는 장'(leaky gut) 가설은 장 세균의 질병 유발 과정을 설명하는 이론적 틀로 널리 알려졌다. 해로운 세균이 장을 벗어나 갖가지 질병으로 이어지는 만성 염증 반응을 촉발한다는 게 이 가설의 핵심이다. 그동안 풀리지 않았던 미스터리는 따로 있다. 어떻게 해서 장을 탈출한 병원성 세균이 수십 년간 숨어 지내느냐 하는 것이다. 실제로 이런 세균은 사람의 몸 안에 오래 머물면서 건강에 아무런 문제도 일으키지 않는다. 마침내 의학계의 이런 해묵은 의문을 풀 수 있는 연구 결과가 나왔다. 연구진은 '숙주 내 진화'(within-host evolution) 현상을 틀로 삼아 어떻게 장 세균이 다른 기관에 질병을 일으키는지 설명했다. 장 세균이 장기간의 진화를 거쳐 장의 방어벽을 넘어가는 능력을 갖추면 병원성이 더 강한, 다시 말해 질병을 일으킬 위험이 더 큰 세균으로 변한다는 게 요지다. 이런 세균은 장 밖의 다른 기관으로 이동한 뒤 면역계 감시망을 피해 숨어 있
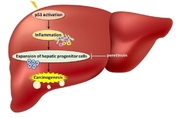
암을 연구하는 생물학 분야에서 p53은 가장 중요한 단백질로 꼽힌다. 일종의 '전사 조절' 단백질인 p53은 DNA 손상과 같은 세포 스트레스 요인에 반응해 활성화한다. p53이 활성화하면 세포 예정사 프로그램 등 다양한 생리 과정이 뒤따라, DNA 손상 등이 생긴 비정상 세포가 암으로 변하는 게 억제된다. p53에 '유전체의 수호자'(guardian of the genome)라는 별칭이 붙은 이유가 여기에 있다. 간세포 암종(hepatocellular carcinoma) 등 여러 유형의 암에서 p53의 돌연변이가 흔히 발견되는 것도 같은 맥락으로 이해된다. 그런데 만성 간 질환(CLD) 환자의 간세포에 p53이 지속해서 활성화하면 간암의 발생을 촉진할 수 있다는 연구 결과가 나왔다. 유독 만성 간 질환에 대해선 p53이 알려진 것과 정반대로 작용한다는 의미다. 일본 오사카대 과학자들이 수행한 이 연구 결과는 12일(현지 시각) 미국 암 연구 협회 저널 '캔서 리서치'(Cancer Research)에 논문으로 실렸다. 1941년 창간된 이 저널은 암과 관련 생물 의학 연구를 다루는 '동료 심사'(peer review) 의학 학술지다. 만성 간 질환은 바이러스
지방 하면 보통 에너지원을 저장하는 백색 지방을 생각한다. 하지만 갈색 지방은 백색 지방을 태워 열을 방출한다. 당연히 갈색 지방은 비만 등의 억제에 도움이 된다. 인간을 비롯한 대부분의 포유류는 진화 과정에서 갈색 지방세포의 발열 메커니즘을 발달시켰다. 추운 환경에서 생존하려면 체온 유지가 필요했다. 그런데 지구의 기온이 상승하면서 점차 이 메커니즘이 필요 없게 됐다. 환경 변화는 갈색 지방세포에 심한 스트레스 요인이 된다. 노화 등이 가세해 스트레스가 심해지면 갈색 지방세포는 발열 기능을 멈추고 스스로 소멸하는 '세포 예정사'(apoptosis)의 길로 들어선다. 신생아 때 체중의 5%이던 갈색 지방이 성장 과정에서 0.1%까지 주는 이유가 여기에 있다. 그래도 비만을 연구하는 과학자들은 갈색 지방세포에 관심이 많다. 갈색 지방을 자극해 지방 연소(발열)를 늘리는 치료가 가능하다고 보는 것이다. 마침내 독일 과학자들이 유력한 해법을 찾아냈다. 죽어가는 갈색 지방세포가 뉴클레오타이드의 일종인 '이노신'(inosine)을 다량 분비해 주위 지방세포의 발열을 자극하는 메커니즘을 발견한 것이다. 푸린(purine) 대사에 관여하는 이노신이 이렇게 풀리면 백색 지
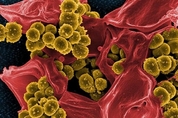
대부분의 경우 황색포도상구균(Staphylococcus aureus)은 흔하고 무해한 세균이다. 숙주인 인간의 몸 안에 함께 살지만, 아무런 해를 끼치지 않는다. 그런데 인간의 면역력이 약해지면 문제를 일으킬 수 있다. 피부, 혈액 등에 침입하는 기회감염 병원체(opportunistic pathogen)로 돌변하는 것이다. 이 병원균의 감염이 진짜 심각해진 건 항생제가 잘 듣지 않는 '다제내성균'(일명 슈퍼버그)이 급속히 퍼지면서부터다. 일례로 슈퍼버그의 동의어처럼 쓰이는 MRSA는 '메티실린 내성 황색포도상구균'(methicillin-resistant Staphylococcus aureus)의 영문 머리글자다. 코로나 팬데믹(대유행)으로 관심이 쏠려 있긴 하지만, 사실 MRSA도 세계 보건 의료계가 직면한 심각한 위협 가운데 하나다. 올해 나온 한 연구 보고서에 따르면 2019년 한해에만 전 세계에서 수천만 명이 항생제 내성균에 감염되고 약 120만 명이 목숨을 잃었다. 이 해에도 감염의 확산과 사망자 발생을 주도한 게 바로 MRSA였다. 특히 MRSA는 병원, 요양소 등 의료 시설 내 감염의 주범으로 꼽힌다. MRSA 확산을 차단하는 가장 효과적인 방법이
코로나 팬데믹(대유행)을 몰고 온 신종 코로나바이러스는 인간의 뇌에 침입하지 못하는 것으로 알려져 있다. 그런데 이 바이러스 감염증(코로나19)에 걸린 환자 중 상당수는 여러 유형의 신경계 질환을 겪는다. 바이러스가 침입하지 못하는데 뇌 조직이 손상되는 희한한 일이 벌어지는 것이다. 이처럼 이율배반적인 현상이 어떻게 일어나는지를 미국 NIH(국립 보건원) 과학자들이 밝혀냈다. 신종 코로나바이러스 감염에 맞서 면역 반응으로 생성되는 항체가, 강력한 필터 역할을 하는 뇌의 '혈뇌장벽'(blood-brain barrier) 혈관에 염증을 일으키는 것으로 밝혀졌다. 뇌혈관을 손상하는 건 바이러스가 아니라, 면역계가 바이러스를 공격하기 위해 만든 항체라는 뜻이다. 이 발견은 코로나19에 수반하는 신경계 질환은 물론이고 이른바 '롱 코비드'(Long COVIDㆍ코로나 후유증)의 유사 증상을 치료하는 데도 큰 도움이 될 거로 보인다. 이 연구는 NIH 산하 NINDS(국립 신경질환 뇌졸중 연구소)의 임상 디렉터인 아빈드라 나스 박사팀이 수행했다. 관련 논문은 5일(현지 시각) 신경학 저널 '브레인'(Brain)에 실렸다. 영국 옥스퍼드대 출판부(Oxford Univers
한 사람의 장(腸)에는 500 내지 1천 종의 미생물종이 존재한다. 장 미생물의 개체 수는 10만 조에 달할 거로 추정된다. 셀 수 없이 많다는 의미다. 장의 미생물종이 균형을 맞춰 공존하는 건 몸뿐 아니라 정신 건강에도 매우 중요하다. 이 균형이 깨지면 무엇보다 몸 안의 대사 체계에 혼란이 생겨 비만, 2형 당뇨병 등 여러 가지 질병이 올 수 있다. 그런데 음식을 한꺼번에 너무 많이 먹거나 먹는 시간이 불규칙하면 장 미생물의 균형에 큰 충격을 준다는 연구 결과가 나왔다. 장의 미생물은 24시간 주기의 '생체시계'(circadian clock)에 맞춰 순환적 변화를 반복했고, 과식이나 나쁜 음식 섭취 패턴은 이 리듬을 교란했다. 미국 샌디에이고 캘리포니아대(UCSD) 의대의 아미르 자린파 조교수팀이 수행한 이 연구 결과는 5일 저널 '셀 리포트'(Cell Reports)에 논문으로 실렸다. 자린파 교수는 UC 샌디에이고 메디컬 센터의 위장병 전문의이기도 하다. 연구팀은 생쥐 모델의 회장(回腸ㆍileum)에 집중했다. 소장(small intestine)의 끝 부위인 회장은 길게 뻗은 구조로 대장이 시작되는 부분과 연결된다. 소장은 위의 소화 작용으로 액화된 음
원래 인간의 간(肝)은 놀라운 재생 능력을 갖췄다. 간의 70%를 잘라내도 수개월만 지나면 남은 조직이 원래 크기로 자랄 수 있다. 간의 이런 복원력을 의학적으로 이용할 수 있다면 고치기 어려운 간 질환에 대한 치료 옵션(선택)도 다양해질 게 분명하다. 의료계의 이런 숙원을 푸는 데 큰 도움이 될 수 있는 획기적인 연구 결과가 나왔다. 간의 재생 단계를 전보다 더 세부적으로 추적할 수 있는 간 혈관 모델이 개발된 것이다. 연구팀은 이 모델을 활용해 생쥐 등 동물 모델 연구에선 접근도 어려웠던 인간 간 조직의 재생 메커니즘을 밝혀냈다. 미국 매사추세츠 공대(MIT) 의료공학 과학 연구소의 산기타 바티아 석좌교수팀이 수행한 이 연구 결과는 최근 미국 국립과학원회보(PNAS)에 논문으로 실렸다. 그는 MIT의 코흐 통합 암 연구소에서도 연구 활동을 하고 있다. 미국 과학진흥협회(AAAS) 사이트(www.eurekalert.org)에 공개된 논문 개요 등에 따르면 간 이식이 필요한 사람은 대부분 바이러스 간염, 지방간, 간암 등의 만성 질환을 앓고 있는 환자다. 간의 재생을 자극하는 확실한 치료법이 있다면 간 이식까지 가지 않아도 될 환자가 적지 않다. 이런 재생
바이러스가 숙주 내에서 증식하려면 계속 에너지를 구해야 한다. 코로나 팬데믹(대유행)을 일으킨 신종 코로나바이러스도 예외는 아니다. 그런데 신종 코로나바이러스가 인체의 지방 처리 시스템을 대대적으로 개편해 입자 복제에 필요한 에너지를 축적하는 것으로 밝혀졌다. 특히 신종 코로나는 트라이글리세라이드(triglyceride)를 좋아했다. 인간도 에너지를 생성하는 데 이 중성 지방을 많이 쓴다. 신종 코로나에 감염되면 체내 지방으로 에너지를 생성하는 능력이 약해진다는 의미일 수 있다. 과학자들은 시중에 판매 중인 비만 치료제와 새로 찾아낸 실험 화합물을 테스트해 신종 코로나바이러스의 복제가 억제된다는 걸 확인했다. 이 발견이 신종 코로나 감염증(코로나19) 치료제 개발의 표적이 될 수 있다는 걸 시사한다. 미국 오리건 보건 과학대(OHSU)의 피카두 타페스 분자 미생물학 교수팀이 수행한 이 연구 결과는 최근 저널 '네이처 커뮤니케이션'(Nature Communications)에 논문으로 실렸다. 이 연구엔 미국 에너지부 산하 '퍼시픽 노스웨스트 국립 연구소'(Pacific Northwest National Laboratory) 과학자들도 참여했다. 미국 과학진흥협
흔히 '에이즈'(AIDS)로 통하는 '후천성 면역결핍 증후군'은 HIV 바이러스에 감염돼 발병하는 전염병이다. 그러나 HIV에 감염됐다고 해서 곧바로 에이즈로 발병하는 건 아니다. 그냥 HIV 감염 상태인 사람은 에이즈 환자와 구분해 'HIV 감염인'이라고 한다. 에이즈에 대한 공포감은 매우 무뎌졌지만, 에이즈를 완치하는 보편적인 치료법은 아직 개발된 게 없다. 다만, 1995년에 나온 고활성 항레트로바이러스 치료법(HAART)은 많은 에이즈 환자의 생명을 구했다. HAART는 NRTI(뉴클레오타이드 유사 역전사 효소 억제제) 등 몇 가지 항바이러스 제제를 병행 투여하는 '칵테일 요법'이다. 완치는 못 해도 중증 진행은 막는 이 치료법의 등장은 에이즈에 대한 인식을 뿌리부터 바꿨다. 요즘 에이즈를 '죽음에 이르는 병'이라고 생각하는 사람은 많지 않다. 적어도 일반인의 인식에서 에이즈는 이제 당뇨병 같은 만성 질환이 됐다. 그런데 HIV 감염의 숨겨진 위험을 알리는 연구 결과가 나왔다. HIV에 감염되면 그 자체로 노화가 빨라져 수명이 5년가량 단축된다는 게 요지다. HIV는 노화와 연관된 생물학적 과정을 재촉하는 것으로 밝혀졌다. 이번 연구는 피험자에 따라