![혈뇌장벽<br>
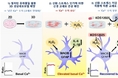
뇌의 혈뇌장벽을 구성하는 모세혈관 내피세포(적색)와 주변세포(녹색).<br>
혈뇌장벽은 뇌혈관과 뇌 조직의 안정성을 유지하는 데 매우 중요한 역할을 한다.<br>
[막스 플랑크 연구소 B. Sheikh 제공 / 재판매 및 DB 금지]](http://www.hmj2k.com/data/photos/20220834/art_16614227157164_6e33e6.jpg)
치매를 유발하는 알츠하이머병이 발달할 때 처음 나타나는 건 아밀로이드 베타(Amyloid beta) 단백질의 침적이다.
알츠하이머병 치료제를 개발하는 과학자들은 오래전부터 이 단백질에 매달렸다.
뇌의 인지 기능이 약해지기 전에 이 단백질을 없애면 알츠하이머병의 예방 또는 치료가 가능하다고 믿었다.
아쉽게도 아밀로이드 베타의 제거는 고사하고 효과를 기대할 만한 어떤 치료법도 아직 개발된 게 없다.
그러던 차에 아밀로이드 베타를 빠르게 청소하는 유전자 신호 경로가 뇌의 단백질 합성 시스템에서 발견됐다.
연구팀은 이 경로를 조절하는 데 효능을 보이는 식물성 천연물과 화합물도 찾아냈다.
이런 물질을 투여한 생쥐는 뇌에 쌓인 아밀로이드 베타를 훨씬 더 빨리 제거했고, 그 효과로 독성 단백질의 침적도 멈췄다.
미국 세인트루이스 워싱턴대의 조지프 도허티 유전학 교수팀이 수행한 이 연구 결과는 24일(현지 시각) 저널 '브레인'(Brain)에 논문으로 실렸다.
도허티 교수팀은 '번역초과 전사'(readthrough)라는 특이한 신호 경로에서 실마리를 찾았다.
우리 몸의 단백질 합성 기계는 때때로 멈춰야 할 지점에서 멈추지 못하는데 이를 '번역초과 전사'라 한다.
유전자 발현은 전사와 번역 두 단계로 나뉜다.
세포핵에서 일어나는 전사는 유전자의 DNA 템플릿(형판)에서 mRMA 분자가 생성되는 과정을 말한다.
번역은 단백질을 합성하는 아미노산 서열을 mRNA로부터 만드는 것인데 핵 바깥의 세포질에서 이뤄진다.
연구팀은 뇌에서 합성되는 아쿠아포린-4(aquaporin 4)라는 단백질에 주목했다. 아쿠아포린은 물의 수송을 담당하는 세포막 단백질이다.
이 단백질도 마찬가지로 긴 사슬 구조의 말단에 조그만 꼬리가 달린 형태로 종종 발견됐다.
처음엔 단백질 합성 과정의 단순한 오류로 치부했다. 다시 말해 '번역초과 전사'의 결과물로 본 것이다.
하지만 아쿠아포린-4처럼 '번역초과 전사'로 말단이 길어진 단백질은 기능이 달라지기도 한다.
몸 안에서 단백질이 합성되는 기본 메커니즘을 생각해도 아쿠아포린-4의 꼬리는 범상치 않았다.
그래서 유전자 염기서열을 분석해봤다. 여기서 '번역초과 전사' 경로가 모든 종에 보존돼 있다는 게 확인됐다.
이 경로는 특히 뇌에서 두드러지게 작동했다. 그런데 특이하게도 노폐물 제거에 중요한 역할을 하는 구조에만 존재했다.
'번역초과 전사' 경로를 표적으로 삼으면 알츠하이머병뿐 아니라 파킨슨병 등 다른 신경 퇴행 질환에도 효과적일 수 있다는 뜻이다.
이런 퇴행성 신경질환의 공통점은 독성 단백질이 뇌에 많이 쌓인다는 것이다.
결정적 진전은 그 다음 단계에 이뤄졌다.
중추신경계 면역세포 중 하나인 성상교세포(astrocyte)의 '종말 단추'(endfeet)에서 꼬리 달린 아쿠아포린-4 단백질을 발견한 것이다.
'종말 단추'는 단추처럼 보이는 '무수(無髓)신경섬유'의 말단으로 다른 신경섬유의 수상돌기와 접합한다.
성상교세포의 주 임무는 신체의 다른 부분으로부터 뇌를 보호하는 '혈뇌장벽'을 정상으로 관리하는 것이다.
성상교세포의 '종말 단추'는 뇌의 미세한 혈관을 감싸고 혈류 조절을 돕는다.
독성 단백질 등 뇌의 노폐물을 바깥의 혈류로 배출하는 완벽한 위치에 자리 잡은 게 바로 성상교세포의 '종말 단추'인 것이다.
연구팀은 꼬리 달린 아쿠아포린-4를 늘리면 뇌의 노폐물 제거를 촉진할 수 있다는 생각에 2천560종의 후보 물질을 스크린했다.
아쿠아포린-4 유전자의 '번역초과 전사'를 활성화하는 작용물질이 필요했다.
복잡하고 까다로운 작업 끝에 후보 물질 2개를 찾아냈다.
하나는 캐모마일, 파슬리, 양파, 토마토, 사과 등에 함유된 플라본(식물체의 황색 색소) 계열 천연물 '아피제닌'(apigenin)이고, 다른 하나는 가축용 항균제 '설파퀴녹살린'(sulfaquinoxaline)이다.
많은 아밀로이드 베타가 뇌에 침적한 생쥐에 실험한 결과, 두 물질 모두 뛰어난 효능을 보였다.
아피제닌이나 설파퀴녹살린을 투여한 생쥐는 대조군(비활성 액체 또는 플라시보<僞藥> 투여)보다 확연히 빠른 속도로 아밀로이드 베타를 제거했다.
아밀로이드 베타는 뇌에서 20∼25%만 줄어도 침적 과정이 중단된다.
이번 생쥐 실험에선 적어도 침적이 멈추는 정도의 아밀로이드 감소가 확인됐다.
이런 효과가 아밀로이드에만 나타난다는 근거는 전혀 없었다.
파킨슨병을 유발하는 알파-시누클레인(alpha-synuclein) 단백질을 제거하는 데도 효과가 있을 거로 과학자들은 예상한다.
단, 설파퀴녹살린은 아직 인간에게 투여했을 때의 안전성이 확인되지 않았다.
아피제닌의 경우 해당 과일이나 야채 등을 통해 보충할 수 있다. 하지만 이렇게 섭취한 아피제닌이 어느 정도 뇌에 도달할지는 미지수다.
연구팀은 알츠하이머병 등의 치료를 목적으로 다량의 아피제닌을 섭취하는 건 자제해야 한다고 경고했다.