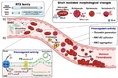
![<strong>HM17321(오른쪽)과 기존 인크레틴 기반 약물의 비만 치료 효능을 비교한 개념도.</strong><br>
[한미약품 제공. 재판매 및 DB 금지]](http://www.hmj2k.com/data/photos/20251040/art_17593144560284_aec0ba.jpg?iqs=0.44523214679189016)
한미약품은 최근 미국 식품의약품청(FDA)에 비만치료제 'HM17321'(LA-UCN2)의 임상 1상 진입을 위한 임상시험계획(IND)을 신청했다고 밝혔다.
HM17321은 글루카곤 유사 펩티드-1(GLP-1)을 비롯한 인크레틴 수용체가 아닌 CRF2 수용체를 선택적으로 타깃하는 우로코르틴(UCN) 2 유사체다.
근육량 증가와 지방 선택적 감량을 동시에 구현하는 세계 최초의 비만 혁신 신약으로 개발되고 있다고 한미약품은 설명했다.
한미약품은 이 치료제 상용화 목표 시점을 2031년으로 설정했다.
최인영 R&D 센터장은 "HM17321은 지방 감량과 근육 증가, 운동 및 대사 기능 개선이라는 통합적 효능을 동시에 지향한다"며 "근감소증 및 고령층 비만, 운동 기능 저하 환자군 등 미충족 수요를 해결할 것"이라고 내다봤다.