
사람들은 보통 병원의 위생 상태가 상대적으로 좋다고 생각한다. 대개는 병원에 가서 나쁜 병원체에 감염될 거로 생각하지 않는다. 하지만 현실은 그렇지 않다. 병원 내 감염은 보건 의료계의 심각한 위협이 된 지 오래다. 미국에선 한해 약 170만 명이 병원에서 감염되고 이 가운데 약 10만 명이 감염 합병증으로 생명을 잃는다. 여기에 들어가는 직접 비용만 300억 달러에 달할 거로 추정된다. 병원 내 감염의 주범은 의료 기기다. 실제로 약 3분의 2가 의료 기기 감염이다. 예를 들면 카테터(catheterㆍ소변 등을 뽑아내는 삽입 도관), 스텐트(stentㆍ혈관을 넓히는 내관), 인공 심장 판막(heart valve), 심박 조율기(pacemaker) 등이 모두 해당한다. 이런 기기를 몸 안에 넣으면 그 표면이 해로운 바이오 필름(biofilm), 즉 미생물 막(세균막)으로 뒤덮인다. 이런 세균막은 물이 닿는 표면이면 어디나 생길 수 있다. 구강 내 치아 플라크(치태)도 일종의 세균막이다. 문제는 끈끈한 바이오 필름이 세균의 온상이라는 것이다. 바이오 필름의 보호를 받으며 공생하는 세균은 항생제, 세정제, 강산성 용액 등에 잘 죽지 않아 다양한 질병의 원인이 된
보통 심혈관계에 위험 요인이 있으면 치매에 걸릴 위험도 커지는 것으로 알려졌다. 그런데 50대 중반 이후엔 고혈압, 당뇨병, 뇌졸중 등의 혈관 위험 요인 가운데 어떤 게 있는지에 따라 치매 위험이 크게 달라진다는 연구 결과가 나왔다. 먼저 55세 전후엔 당뇨병과 고혈압이 향후 10년 내 치매에 걸릴 위험을 높였다. 또 65세 땐 심장 질환이, 70세 땐 당뇨병과 뇌졸중이 그랬다. 80세 땐 당뇨병과 뇌졸중 병력을 가진 사람이 치매에 더 많이 걸렸다. 스웨덴 우메오 대학(Umea University) 과학자들이 주도한 이 연구 결과는 18일(현지 시각) 미국 신경학회 저널 '신경학'(Neurology) 온라인판에 논문으로 실렸다. 이 대학 과학자들은 미국 매사추세츠주 소재 프레이밍햄 연구소가 진행한 '심혈관 코호트(같은 특성을 가진 집단) 장기 연구'(Framingham Heart Study) 데이터를 분석했다. 연구가 시작될 때 55세 전후의 주민 4천899명이 참가했다. 이 가운데 80세가 될 때까지 치매 증상을 전혀 보이지 않은 사람은 48.7%인 2천386명이었다. 연구팀은 65세부터 치매가 생겼는지 추적했다. 55세 때 당뇨병인 사람은 10년 안에 치
코로나19(신종 코로나바이러스 감염증) 환자에겐 '브레인 포그'(Brain fog), 두통, 불면증 등의 신경 증상이 나타날 수 있다. '브레인 포그' 증후군은 머릿속에 안개가 낀 것처럼 집중이 잘 안 되고 멍한 상태가 지속하는 걸 말한다. 이런 유형의 바이러스 감염 후유증은 이번 코로나 팬데믹(대유행)에서 처음 겪는 일이 아니다. 사실 1918년 인플루엔자(독감) 팬데믹 때도 그런 일이 있었다. 하지만 당시엔 거의 10년이 지나서야 다수의 파킨슨병 환자가 보고됐다. 이처럼 바이러스 감염으로 중뇌 기저핵(basal ganglia)의 도파민 분비 세포가 소멸하는 질환을 '포스트 뇌 파킨슨병'(post-encephalic parkinsonism)이라고 한다. 지금까진 몸 안에 침입한 바이러스가 어떤 메커니즘을 통해 뇌 조직을 손상하는지 잘 몰랐다. 그런데 신종 코로나바이러스가 파킨슨병 발생 위험을 높일 수 있다는 연구 결과가 나왔다. 파킨슨병과 유사한 패턴의 뇌 조직 퇴행이 코로나19 환자에게 일어난다는 것이다. 이 연구는 미국 토머스 제퍼슨 대학 과학자들이 수행했다. 논문은 '국제 파킨슨병 운동 장애 협회'가 발행하는 임상 신경학 저널 '운동 장애'(Movem

유전적 요인은 생활 양식(lifestyle)이나 환경 못지않게 비 감염 질환의 원인이 된다. 암은 물론이고 심혈관 질환, 염증 질환 등에 걸릴 개인별 위험이 이런 요인들에 의해 많이 달라진다. 유전역학자들은 오래전부터 질병 등의 '유전 가능성'(heritability)을 연구해 왔다. 다시 말하면 부모의 특정 성향이 유전자를 통해 자녀에게 전해지는 정도와 범위를 탐구해온 것이다. 극적인 돌파구를 연 게 '전장 유전체 연관 분석'(GWAS) 기술이다. 이 기술이 등장한 이후 일반적 질병이나 건강 관련 성향에 관여하는 수천 종의 유전자 변이가 짧은 기간에 확인됐다. 최근의 DNA 분석기술은 인간의 유전체에서 변이가 생긴 위치를 개인별로 확인하는 수준까지 발전했다. 지금까지 유전적 변이의 압도적 다수는 소수의 사람에게 드물게 생기는 것이고, 어떤 경우엔 특정 집단에 국한되는 것으로 알려졌다. 그런데 대부분의 유전병은, 작용 범위가 넓지 않은 다수의 흔한 유전자 변이가 조합해 생긴다는 연구 결과가 나왔다. 반대로 희소한 유전자 변이는 해당하는 소수의 사람에게만 질병 위험을 높이는 것으로 나타났다. 이전의 유전자 연구가 유전자의 질병 유발 효과를 상당히 많이 간과했을
나쁜 식습관이 암을 부르고 암의 진행에도 나쁜 영향을 미친다는 가설은 오래전부터 존재했다. 마침내 이 가설이 사실이라는 걸 강력히 시사하는 연구 결과가 나왔다. 음식물에 포함된 지방의 양과 몸 안의 산화질소(Nitric oxide) 수위 사이에 분명한 연관성이 있다는 게 과학적 실험을 통해 입증된 것이다. 산화질소는 암의 발달, 염증 발생 등에 관여하는 신호 분자다. 미국 일리노이대 어배너-섐페인 캠퍼스의 '베크만 첨단 과학 공학 연구소' 과학자들이 수행한 이 연구 결과는 최근 미국 화학회(ACS)가 발행하는 저널 'ACS 중심 과학'(ACS Central Science)에 논문으로 실렸다. 미국 과학진흥협회(AAAS) 사이트(www.eurekalert.org)에 따르면 연구팀은 종양 미세환경의 미묘한 변화가 분자 수준에서 암의 발달에 어떤 영향을 미치는지 밝히는 데 초점을 맞췄다. 세포는 생존과 성장을 위해 일반 세포와 다른 주변 환경을 조성하는데 이를 종양 미세환경이고 한다. 양 미세환경에 깊숙이 관여하는 요인 중 하나가 바로 염증이다. 구팀은 특히 칼로리가 높고 지방이 많이 함유된 고가공식(highly processed food)에 주목했다. 고가공식이
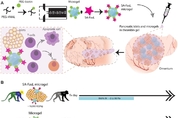
1형 당뇨병은 인슐린을 생성하는 췌장의 베타세포가 자가면역 반응으로 파괴되는 병이다. 이렇게 베타세포가 손상되면 인슐린 부족으로 혈당치가 급격히 치솟아 치명적인 결과를 초래할 수 있다. 그래서 1형 당뇨병 환자는 매일 인슐린을 투여해야 한다. 베타세포, 알파세포(글루카곤 생성 세포) 등이 모여 있는 췌장의 랑게르한스섬을 이식하는 게 1형 당뇨병의 유력한 치료법이 될 수 있다. 하지만 이런 세포치료는 거부 반응이 심해, 설사 효과를 본다고 해도 평생 면역억제제에 의존해야 한다. 1형 당뇨병 환자에게 랑게르한스섬을 이식할 때 거부 반응을 피할 수 있는 획기적인 치료 전략이 개발됐다. 간단히 말하면 신종 생체적합 물질(biomaterial)을 랑게르한스섬과 섞어 함께 이식하는 것이다. 면역 억제 단백질이 포함된 이 물질의 작용으로 이식한 랑게르한스섬이 장기간 보존되는 것으 로 확인됐다. 미국 하버드의대의 최대 교육병원인 매사추세츠 제너럴 호스피털(MGH) 과학자들이 주도한 이 연구 결과는 13일(현지 시각) 저널 '사이언스 어드밴시스'(Science Advances)에 논문으로 게재됐다. 이 연구엔 미국 조지아 공대와 미주리대 과학자들도 참여했다. 연구팀은 1형
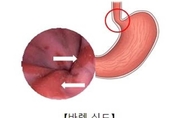
식도의 끝부분이 장기간 역류 위산에 노출되면 위 조직 같이 된다. 위산의 공격에 견디려고 식도 조직이 이렇게 변한 걸 '바렛 식도'(Barrett's esophagus)라고 한다. 위와 식도는 바로 연결되는 장기이긴 하나, 점막을 이루는 세포는 서로 다르다. 다시 말해 식도 점막은 편평상피세포로, 위 점막은 원주상피세포로 구성돼 있다. 바렛 식도가 생기면 가슴 통증 등이 따르지만 당장 큰 문제가 되는 건 아니다. 그런데 바렛 식도 환자의 약 5%는 식도암의 한 유형인 '식도 선암(腺癌'(esophageal adenocarcinoma)으로 진행한다. 게다가 암이 되지 않는 나머지 95%의 바렛 식도 환자까지 식도암 공포에 떨어야 한다. 미국 연구진이 이런 문제를 푸는 해법을 찾아냈다. 바렛 식도 환자에게 어떤 유전적 변이가 생기면 식도암 위험이 커지는지 상세히 밝혀낸 것이다. 종양 억제 유전자로 알려진 TP53의 활성화를 방해하는 돌연변이가 문제였다. 부모로부터 각각 하나씩 받은 두 개의 TP53 카피에 모두 변이가 생기면 특히 발암 위험이 커졌다. 미국 프레드 허친슨 암 연구 센터(Fred Hutchinson Cancer Research Center) 과학자
우리 주변에 복용 약이 흔해도 먹는 방식으론 효과를 보기 어려운 약도 적지 않다. 복용한 약이 위(胃)의 강산성 소화액을 견뎌내고 온전히 소장(小腸)까지 가는 게 쉽지 않기 때문이다. 약이 위에서 많이 분해되면 작용 성분이 소장의 혈관을 통해 충분히 흡수되지 못한다. 약을 먹을 때 필요한 것보다 많은 양을 쓰는 이유도 위를 거치면서 상당한 양이 분해되기 때문이 다. 복용 약의 이런 고질적인 문제를 해결할 수 있는 신종 운반 물질을 미국 과학자들이 개발했다. 위의 산성 환경에 파괴되지 않고 소장에서 잘 분해되는 '양성 이온 중합 복합체'(pZC)를 만들어낸 것이다. 이 물질은 흔한 경구용(經口用) 항생제부터 최신 단백질 치료제까지 거의 모든 유형의 약물 전달에 근본적인 변혁을 가져올 거로 기대된다. 미국 매사추세츠대 애머스트 캠퍼스(University of Massachusetts Amherst) 과학자들이 수행한 이 연구 결과는 최근 저널 '네이처 커뮤니케이션'(Nature Communications)에 논문으로 실렸다. 미국 과학진흥협회(AAAS) 사이트(www.eurekalert.org)에 공개된 논문 개요 등에 따르면 복용 약을 쓰기 어려우면 주사로 약

루푸스병(lupus)은 면역 이상으로 온몸에 염증이 생기는 만성 자가면역질환이다. 우리 말로는 '전신 홍반성 낭창'이라고 한다. 루푸스에 걸리면 장기, 혈관계, 조직 등이 염증으로 손상돼 기능 부전으로 이어진다. 희소 질환이긴 하나, 여성 환자가 남성보다 훨씬 많다. 특히 가임기 여성에게 많이 생기는 경향을 보인다. 루푸스병 환자의 70∼80%는 다른 부위의 염증과 별개로 피부 발진이 나타난다. 이를 따로 '피부 홍반 루푸스'(CLE)라고 한다. 이 유형의 루푸스 환자는 자외선에 민감한 것으로 알려졌다. 실제로 환자의 30∼40%는 장시간 햇빛에 노출될 경우 증상이 악화하는 것으로 보고됐다. 미국 미시간 의대 과학자들이 루푸스병의 숨겨진 비밀을 하나 밝혀냈다. 루푸스병 환자는 발진이 생겼을 때와 똑같은 염증 신호가 정상 피부에도 나타난다는 것이다. 환자에 따라선 정상 피부의 염증 신호가 발진 시보다 훨씬 더 강한 경우도 있었다. 미셸 칼렌버그 류머티스학 부교수팀이 수행한 이 연구 결과는 최근 저널 '사이언스 중개 의학'(Science Translational Medicine)에 논문으로 실렸다. 미국 과학진흥협회(AAAS) 사이트(www.eurekalert.